Em até 12x de R$10,69

Em até 12x de R$10,69










































































ROTEIRO DE AULA PRÁTICA – QUÍMICA E CIÊNCIA DOS MATERIAIS
R$110,00 O preço original era: R$110,00.R$90,00O preço atual é: R$90,00.
Em até 12x de R$10,69
CLIQUE AQUI PARA VISUALIZAR O MANUAL COMPLETO
Este produto refere-se à resolução (resposta) da atividade, fornecida no formato WORD, conforme o formulário padrão da instituição de ensino. O download do arquivo é imediato após a confirmação do pagamento.
⚠️ATENÇÃO: Recomenda-se que o aluno modifique o conteúdo para evitar qualquer forma de cópia. Não nos responsabilizamos por eventuais cópias.
ROTEIRO
Aula Prática
QUÍMICA E CIÊNCIA DOS MATERIAIS
ROTEIRO DE AULA PRÁTICA 1
NOME DA DISCIPLINA: QUÍMICA E CIÊNCIA DOS MATERIAIS
Unidade: U1_ESTRUTURA ATÔMICA
Aula: A4_ESTADO DA MATÉRIA: GASES, LÍQUIDOS E SÓLIDOS
OBJETIVOS
(campo obrigatório – exibição para todos)
Definição dos objetivos da aula prática:
Estabelecer relação entre massa e volume de líquidos.
INFRAESTRUTURA
(OBRIGATÓRIO SE HOUVER – EXIBIÇÃO DOCENTE/TUTOR)
Instalações – Materiais de consumo – Equipamentos:
LABORATÓRIO DE INFORMÁTICA
Equipamentos:
• Computador com acesso à internet
~ 1 unid. / 1 aluno
SOLUÇÃO DIGITAL
(OBRIGATÓRIO SE HOUVER – APARECER PARA TODOS)
Infraestrutura mínima necessária para execução.
Laboratório Virtual Algetec – simulador: “Reação de Neutralização Ácido-Base”.
O laboratório virtual é uma plataforma para simulação de procedimentos em laboratório e deve ser acessado por computador, não deve ser acessado por celular ou tablet. O primeiro acesso ao simulador será um pouco mais lento, pois alguns plugins são buscados no navegador. A partir do segundo acesso, a velocidade de abertura dos experimentos será mais rápida.
O link da atividade prática estará disponível em seu AVA.
EQUIPAMENTO DE PROTEÇÃO INDIVIDUAL (EPI)
(CAMPO OBRIGATÓRIO – APARECER PARA TODOS)
Para a utilização do laboratório de informática não há necessidade de EPI’s.
PROCEDIMENTOS PRÁTICOS
(OBRIGATÓRIO – TODOS)
Procedimento / Atividade nº 1 (Virtual)
MEDIDAS DE MASSA E VOLUME DE LÍQUIDOS
Atividade proposta
Conhecer e identificar os tipos de vidrarias, instrumentos e equipamentos presentes em um laboratório de química, bem como o uso adequado para cada situação, estabelecer o processo de medição de massa e volume dos líquidos.
Procedimentos para a realização da atividade
Esse experimento utilizará algumas vidrarias: pipeta graduada, proveta, béqueres e instrumentos que servirão para auxiliar na execução da prática, como o pipetador de borracha de três vias, comumente chamado de pera, e a pisseta de água destilada.
Para o desenvolvimento do experimento, as medições de volume serão realizadas com diferentes vidrarias e as medições de massa serão realizadas com auxílio de uma balança analítica.
Dessa forma, para a execução da atividade prática, em seu AVA, você irá encontrar o link do experimento MEDIDAS DE MASSA E VOLUME DE LÍQUIDOS, que será desenvolvido na plataforma VirtuaLab da Algetec. A partir do acesso, seguem os procedimentos a serem realizados no laboratório virtual para o desenvolvimento da atividade.
➨ Segurança do experimento
Visualize o armário de EPIs clicando com o botão esquerdo do mouse na câmera “Armário de EPIs”, localizada no canto superior esquerdo da tela, ou utilize o atalho Alt+4.
Abra o armário de EPIs clicando sobre as portas.
Selecione os EPIs necessários para a realização do ensaio. Neste experimento, é obrigatório o uso de jaleco e luvas.
Feche o armário de EPIs clicando sobre as portas.
Visualize as gavetas clicando na câmera “Gavetas” ou utilizando o atalho Alt+2.
➨ Preparando o experimento
Abra a primeira gaveta.
Mova o béquer de 250 mL para a mesa, selecionando “Colocar sobre a mesa”.
Repita o procedimento para o béquer de 50 mL.
Feche a gaveta.
➨ Utilizando a pisseta e o béquer
Visualize a bancada pela câmera “Bancada” ou atalho Alt+1.
Observe a temperatura do laboratório no termômetro e registre o valor.
Posicione a pisseta com água destilada sobre o béquer de 50 mL.
Despeje 10 mL de água.
Retorne a pisseta para a mesa.
Visualize a balança pela câmera “Balança Analítica” ou atalho Alt+3.
➨ Utilizando a função tara da balança analítica
Ligue a balança.
Abra a porta lateral esquerda.
Coloque o béquer de 250 mL na balança.
Feche a porta lateral e registre o valor.
Tare a balança.
➨ Entendendo o uso da pera e da pipeta
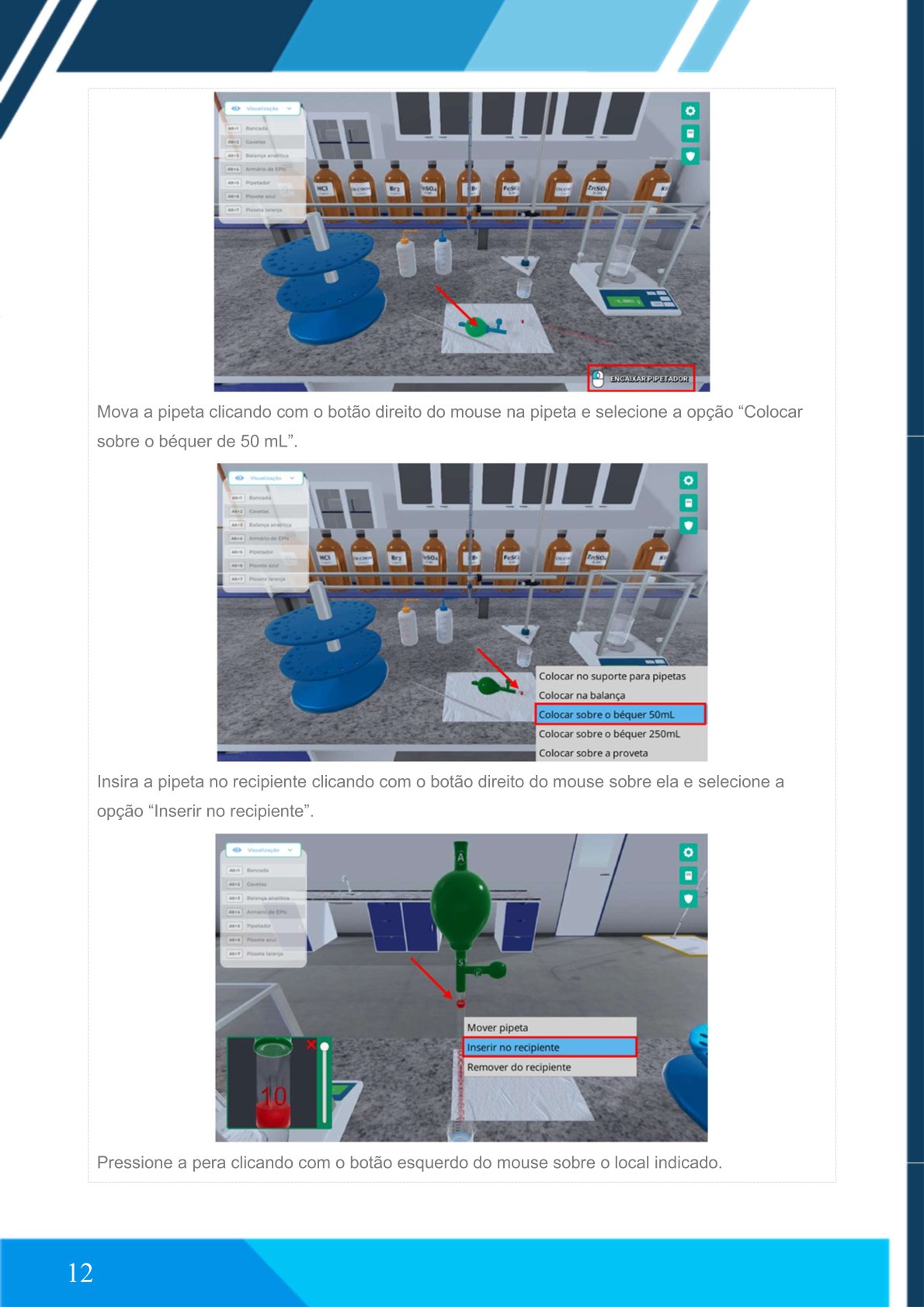
Conecte a pera à pipeta.
Coloque a pipeta sobre o béquer de 50 mL.
Insira a pipeta no recipiente.
Pressione a pera.
Succione o conteúdo pela válvula “S”.
Despeje o conteúdo pela válvula “E”.
➨ Utilizando a pipeta
Succione 10 mL de água.
Ajuste a câmera de graduação.
Retire a pipeta do recipiente.
Visualize a balança analítica.
➨ Medindo a massa de água na pipeta
Abra a porta superior da balança.
Coloque a pipeta na balança.
Despeje o conteúdo.
Coloque a pipeta no suporte.
Feche a porta superior e registre os valores.
Abra a porta lateral.
Retorne o béquer de 250 mL para a mesa.
Descarte o conteúdo dos béqueres de 250 mL e 50 mL.
➨ Medindo com a proveta
Retire a tara da balança.
Coloque a proveta na balança.
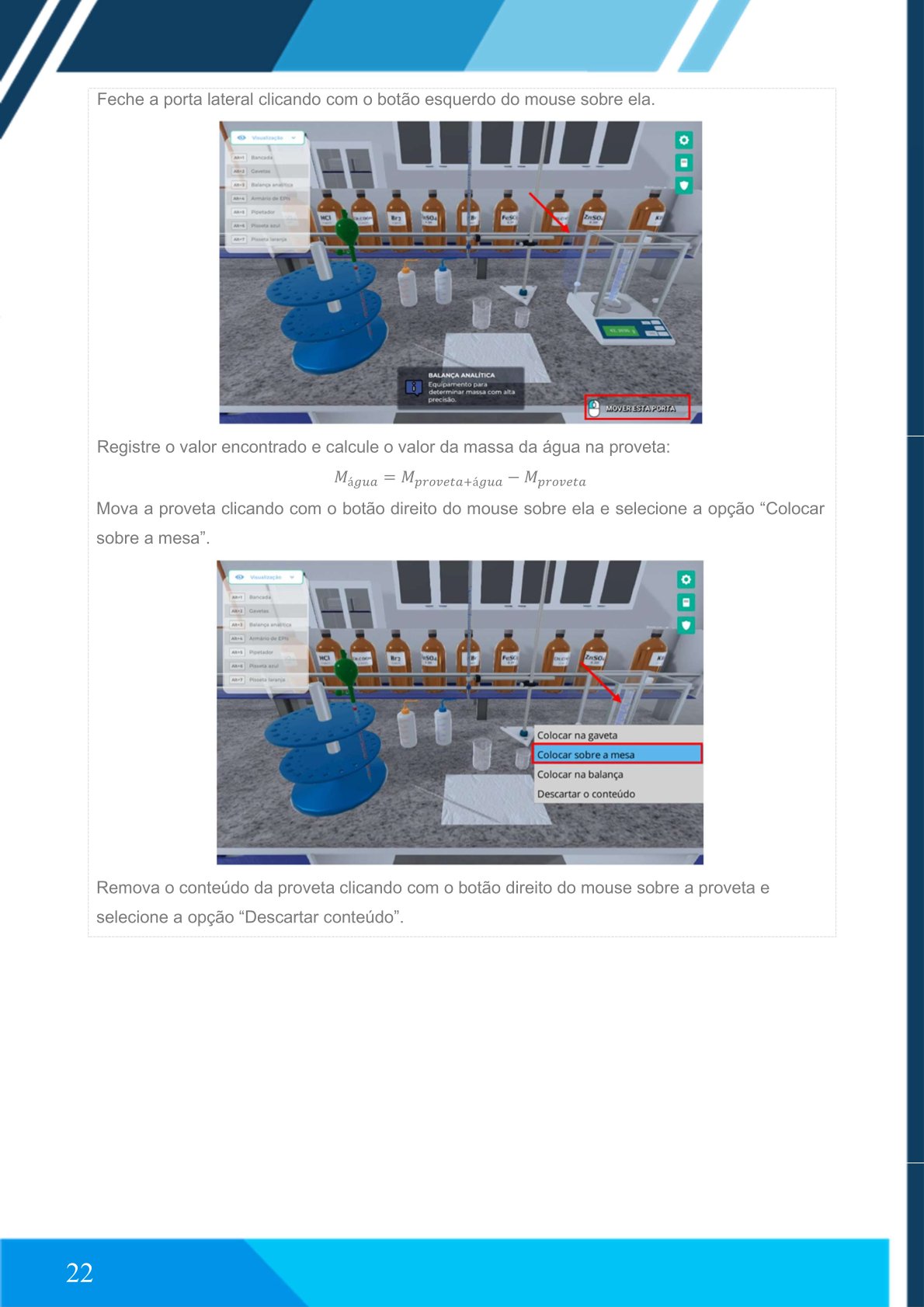
Feche a porta lateral.
Abra a porta lateral e coloque a proveta sobre a mesa.
Posicione a pisseta sobre a proveta.
Deposite 15 mL de água destilada.
Retorne a pisseta à mesa.
Coloque a proveta na balança.
Feche a porta lateral e registre o valor.
Calcule a massa da água na proveta:
mₐ = Mₐ − M
Descarte o conteúdo da proveta.
➨ Calculando a densidade
Coloque o béquer de 50 mL na balança.
Feche a porta lateral e registre o valor.
Abra a porta lateral e coloque o béquer sobre a mesa.
Deposite 15 mL de água destilada no béquer.
Coloque o béquer novamente na balança.
Registre o valor e calcule a massa da água:
mₐ = Mé á − Mé
Determine a densidade da água destilada:
ρ = m / V
Descarte o conteúdo do béquer.
➨ Explorando a precisão das vidrarias
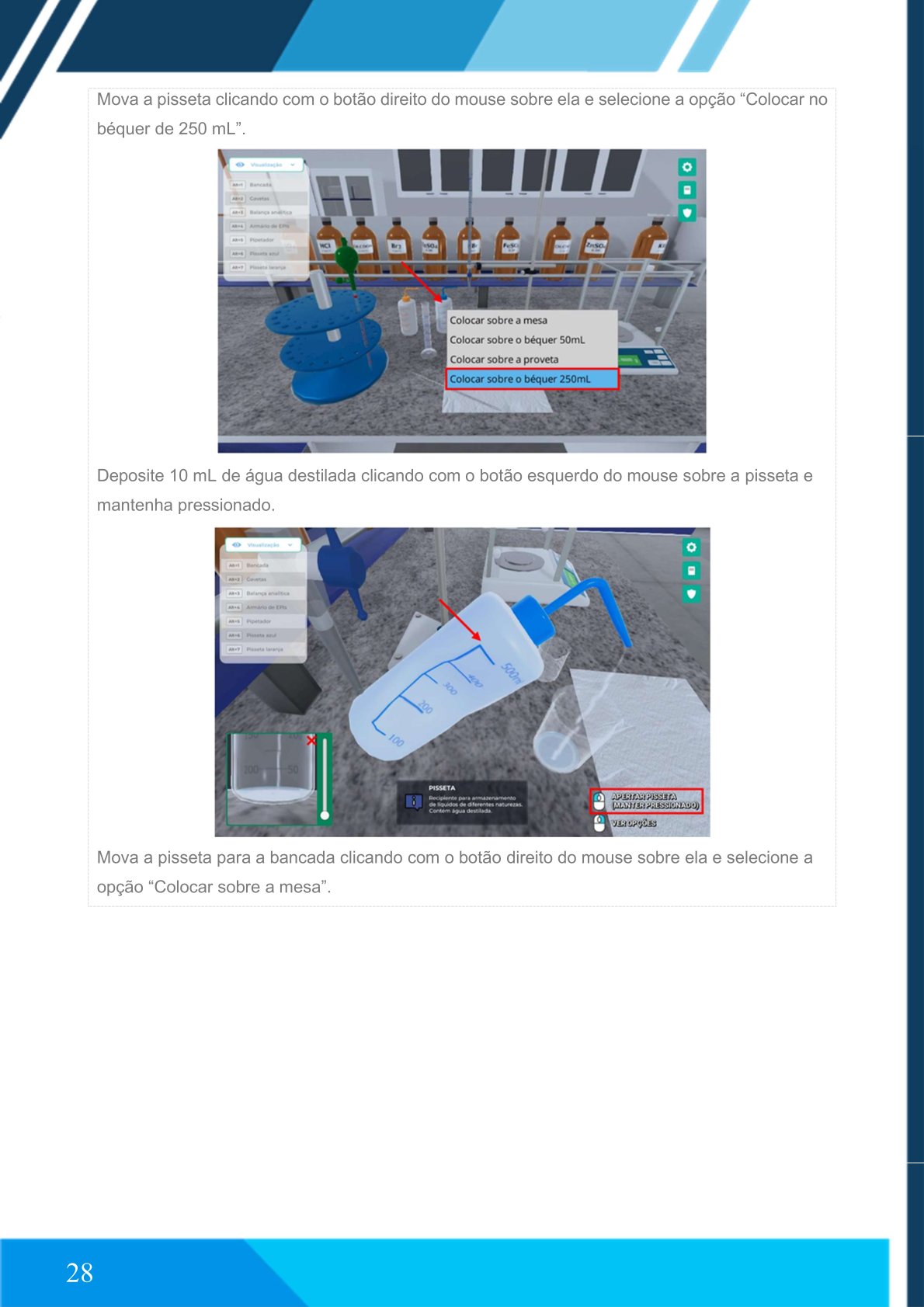
Coloque a pisseta no béquer de 250 mL.
Deposite 10 mL de água destilada.
Retorne a pisseta à mesa.
Coloque a pipeta sobre o béquer de 250 mL.
Retire o ar da pera.
Insira a pipeta no recipiente.
Succione o conteúdo.
Remova a pipeta do recipiente.
Coloque a pipeta no suporte.
Coloque a pisseta na proveta.
Deposite 6,5 mL de água destilada.
MEDIDAS DE MASSA E VOLUME DE LÍQUIDOS
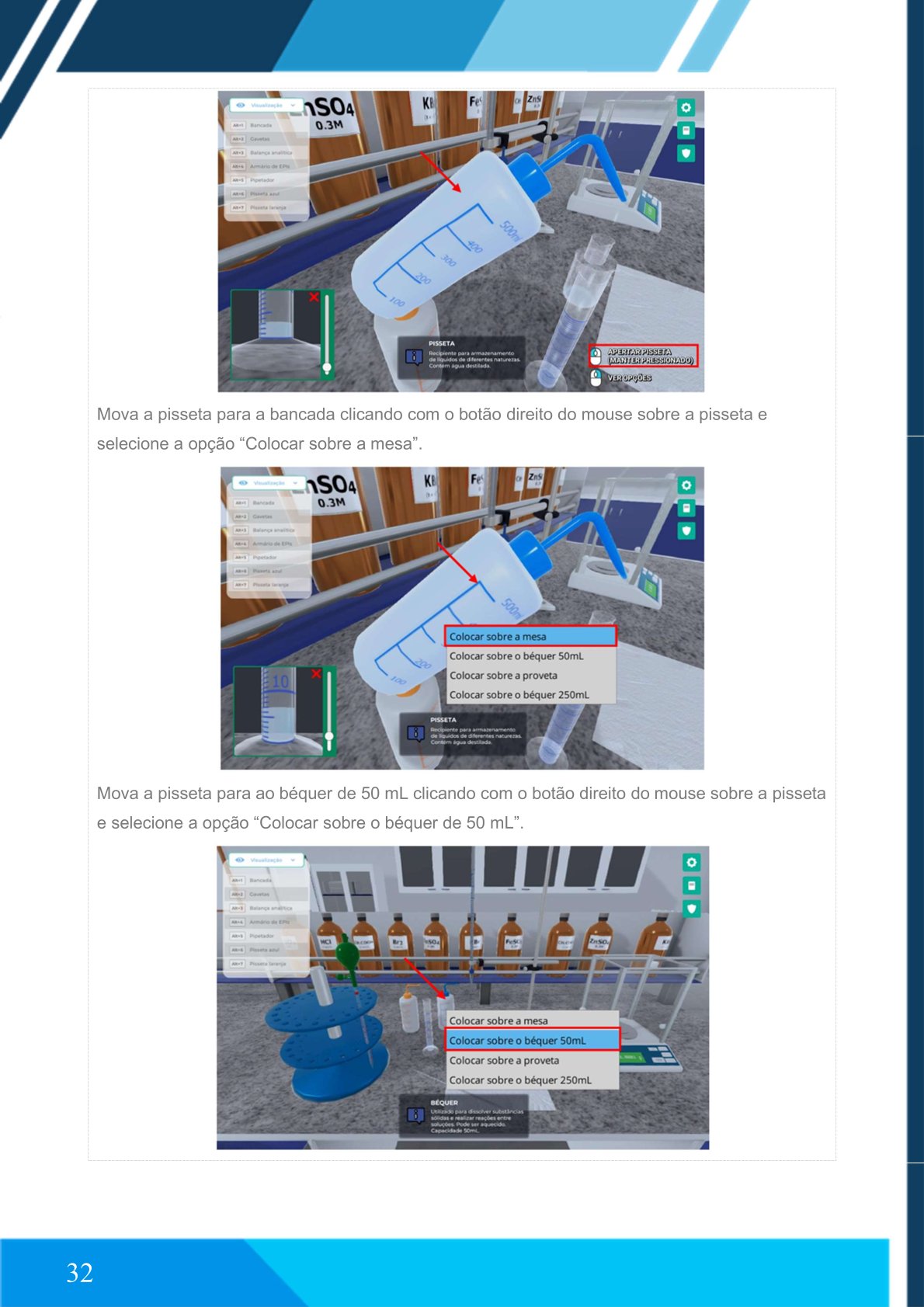
Mova a pisseta para a bancada clicando com o botão direito do mouse sobre a pisseta e selecione a opção “Colocar sobre a mesa”.
Mova a pisseta para o béquer de 50 mL clicando com o botão direito do mouse sobre a pisseta e selecione a opção “Colocar sobre o béquer de 50 mL”.
Despeje 6,5 mL de água clicando com o botão esquerdo do mouse sobre a pisseta e mantenha pressionado.
Retorne a pisseta para a mesa clicando com o botão direito do mouse sobre ela e selecione a opção “Colocar sobre a mesa”.
➨ Finalizando o experimento
Remova o conteúdo das vidrarias clicando com o botão direito do mouse sobre elas e selecione a opção “Descartar conteúdo”.
Visualize as gavetas clicando com o botão esquerdo do mouse na câmera “Gavetas” ou através do atalho Alt+2.
Abra a gaveta indicada clicando com o botão esquerdo do mouse sobre ela.
Visualize a mesa clicando com o botão esquerdo do mouse na câmera “Bancada” ou através do atalho Alt+1.
Guarde as vidrarias clicando com o botão direito do mouse sobre elas e selecione a opção “Colocar na gaveta”.
Desligue a balança analítica clicando com o botão esquerdo do mouse sobre o botão indicado.
➨ Avaliando os resultados
Utilize uma tabela, como a tabela abaixo, para registro dos dados encontrados no experimento.
Vidrarias
Massa de vidraria seca (g)
Proveta 50 mL
Béquer 50 mL
Massa de vidraria + 15 mL de água
Massa dos 15 mL de água
Temperatura (°C)
Com os dados obtidos e calculados, responda:
Com base nos seus conhecimentos, qual a vantagem de tarar a balança com o béquer dentro? Justifique.
Considerando as vidrarias selecionadas, quais seriam as mais indicadas em termos de medição de volumes? Reflita sobre sua resposta.
Checklist
✓ Acessar seu AVA
✓ Clicar no link do experimento MEDIDAS DE MASSA E VOLUME DE LÍQUIDOS
✓ Garantir a Segurança e Preparação do Experimento
✓ Utilizar a pisseta e o béquer
✓ Tarar a balança analítica
✓ Compreender o uso da pera e da pipeta
✓ Utilizar a pipeta
✓ Medir a massa de água na pipeta
✓ Medindo com a proveta
✓ Calculando a densidade
✓ Explorando a precisão das vidrarias
✓ Finalizar o experimento
✓ Avaliar os resultados
RESULTADOS
(obrigatório – aparecer para todos)
Resultados de Aprendizagem:
Como resultados dessa prática será possível utilizar um pipetador de borracha de três vias, saber utilizar as funções principais de uma balança analítica, identificar vidrarias utilizadas em laboratório e compreender suas utilidades, transferir líquidos com volumes diferentes, estabelecer relação entre massa e volume de líquidos. E ainda, conhecer as funcionalidades práticas das ferramentas do laboratório.
ESTUDANTE, VOCÊ DEVERÁ ENTREGAR
(não obrigatório – aparecer para todos)
Ao final dessa aula prática, você deverá enviar um arquivo em Word contendo as informações obtidas no experimento, os cálculos realizados, em conjunto com um texto conclusivo a respeito das informações obtidas.
O arquivo não pode exceder o tamanho de 2 Mb.
REFERÊNCIAS BIBLIOGRÁFICAS
(não obrigatório – aparecer para todos)
Descrição (em ABNT) das referências utilizadas.
ROTEIRO DE AULA PRÁTICA 2
NOME DA DISCIPLINA: QUÍMICA E CIÊNCIA DOS MATERIAIS
Unidade: U2_ESTUDO DE REAÇÕES QUÍMICAS
Aula: A3_REAÇÕES EM SOLUÇÃO AQUOSA
OBJETIVOS
(campo obrigatório – exibição para todos)
Aplicar os conceitos de reações ácido-base para analisar uma reação de neutralização, verificando sua titulação.
INFRAESTRUTURA
(OBRIGATÓRIO SE HOUVER – EXIBIÇÃO DOCENTE/TUTOR)
LABORATÓRIO DE INFORMÁTICA
Equipamentos:
• Computador com acesso à internet
~ 1 unid. / 1 aluno
SOLUÇÃO DIGITAL
(OBRIGATÓRIO SE HOUVER – APARECER PARA TODOS)
Laboratório Virtual Algetec – simulador: “Reação de Neutralização Ácido-Base”.
O laboratório virtual é uma plataforma para simulação de procedimentos em laboratório e deve ser acessado por computador, não deve ser acessado por celular ou tablet. O primeiro acesso ao simulador será um pouco mais lento, pois alguns plugins são buscados no navegador. A partir do segundo acesso, a velocidade de abertura dos experimentos será mais rápida.
O link da atividade prática estará disponível em seu AVA.
EQUIPAMENTO DE PROTEÇÃO INDIVIDUAL (EPI)
(campo obrigatório – aparecer para todos)
Para a utilização do laboratório de informática não há necessidade de EPI’s.
PROCEDIMENTOS PRÁTICOS
Procedimento / Atividade nº 1 (Virtual)
REAÇÃO DE NEUTRALIZAÇÃO ÁCIDO-BASE
Atividade proposta:
Compreender os procedimentos para realizar uma reação de neutralização e como identificar sua titulação.
Procedimentos para a realização da atividade
Em seu AVA, você irá encontrar o link do experimento REAÇÃO DE NEUTRALIZAÇÃO ÁCIDO-BASE, que será desenvolvido na plataforma VirtuaLab da Algetec.
➨ Escolhendo o comprimido para o experimento
Escolha o comprimido de Aspirina®:
Opção 1: aproximadamente 450 mg
Opção 2: aproximadamente 1000 mg
Opção 3: massa aleatória entre 450 mg e 1000 mg
➨ Segurança do experimento
Selecione jaleco, luvas e óculos de proteção no armário de EPIs.
➨ Preparando o experimento
Retire e posicione béquer, proveta e Erlenmeyer.
Separe a fenolftaleína.
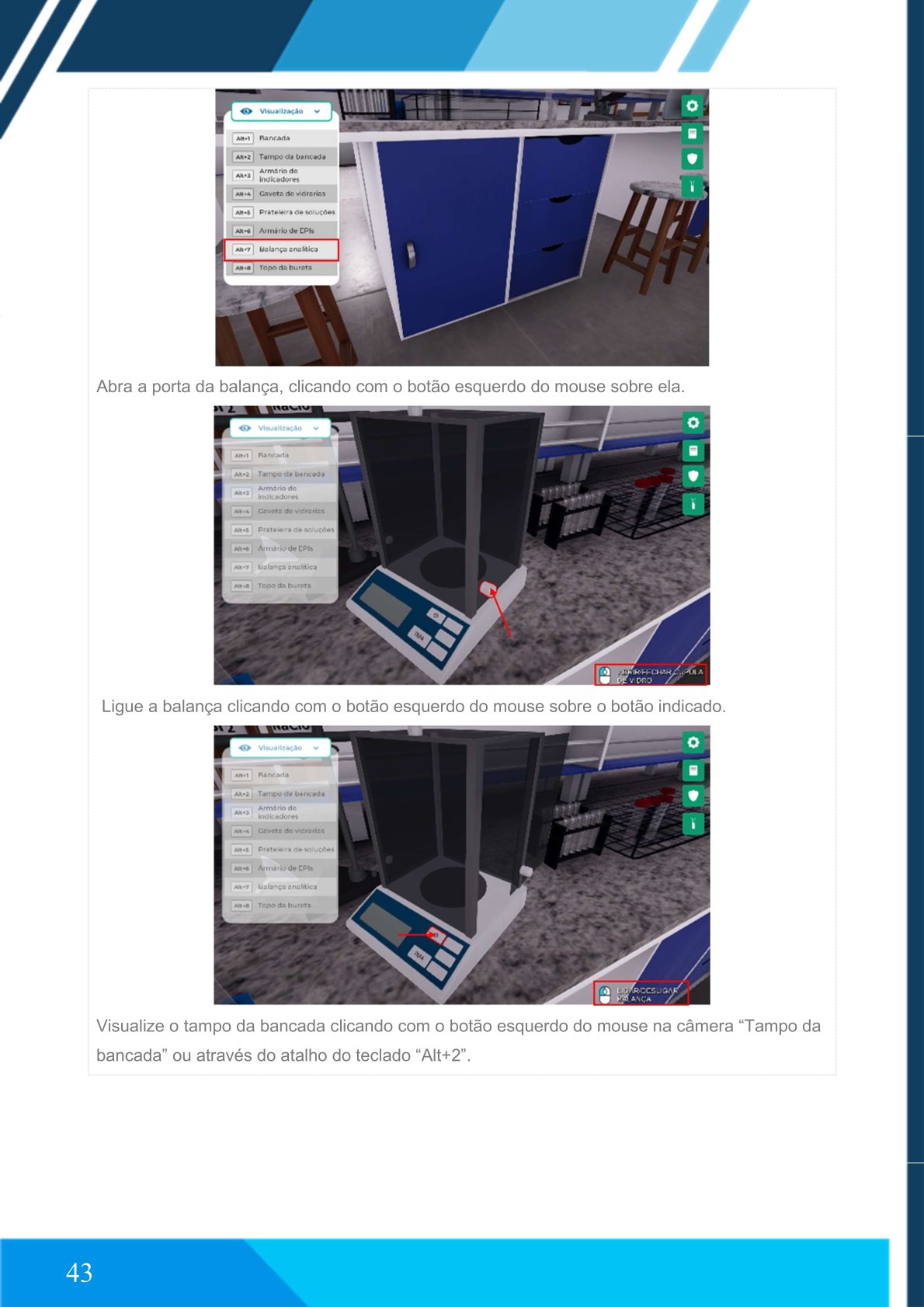
Ligue a balança analítica.
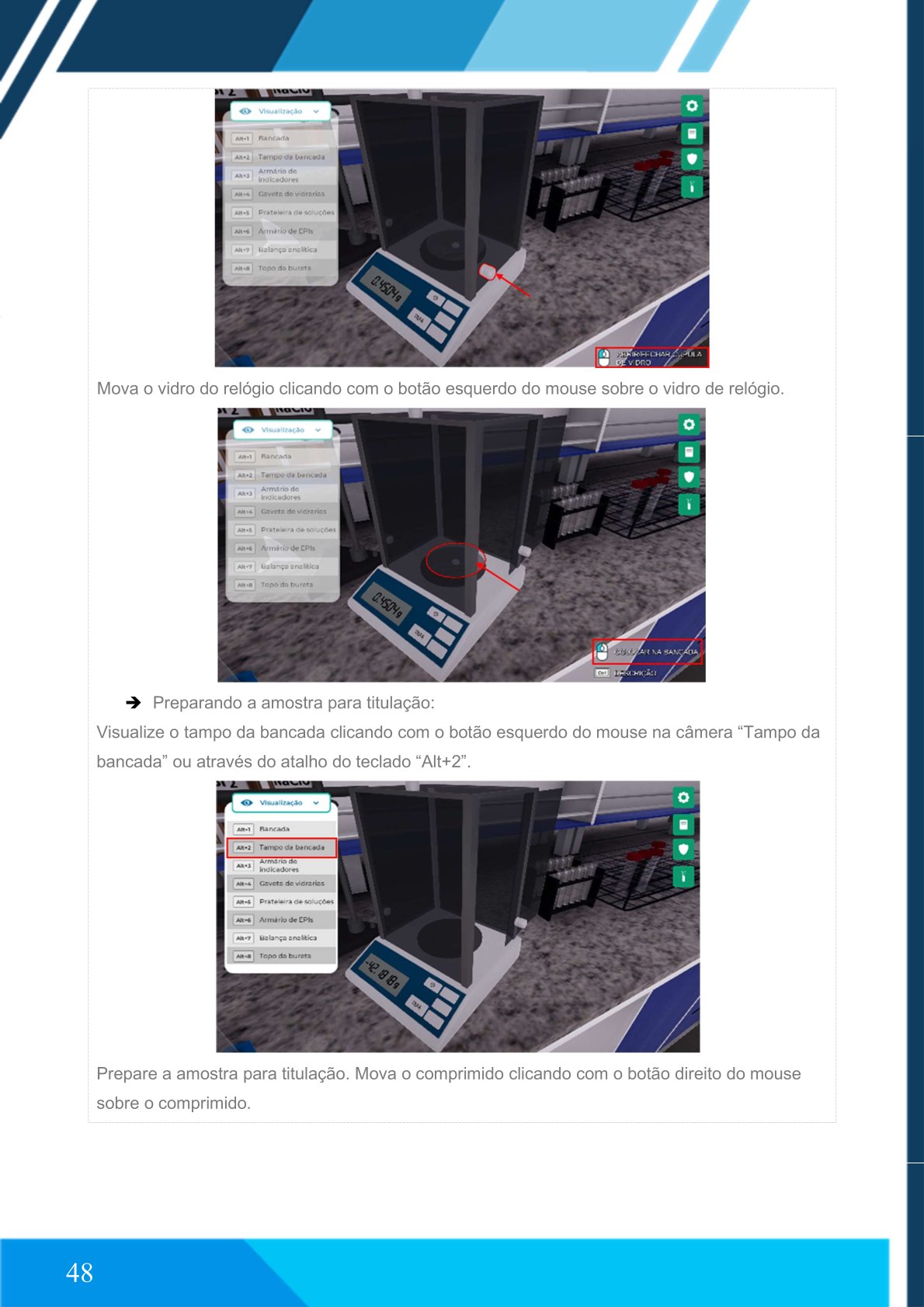
Realize a tara do vidro de relógio.
Pese o comprimido de Aspirina®.
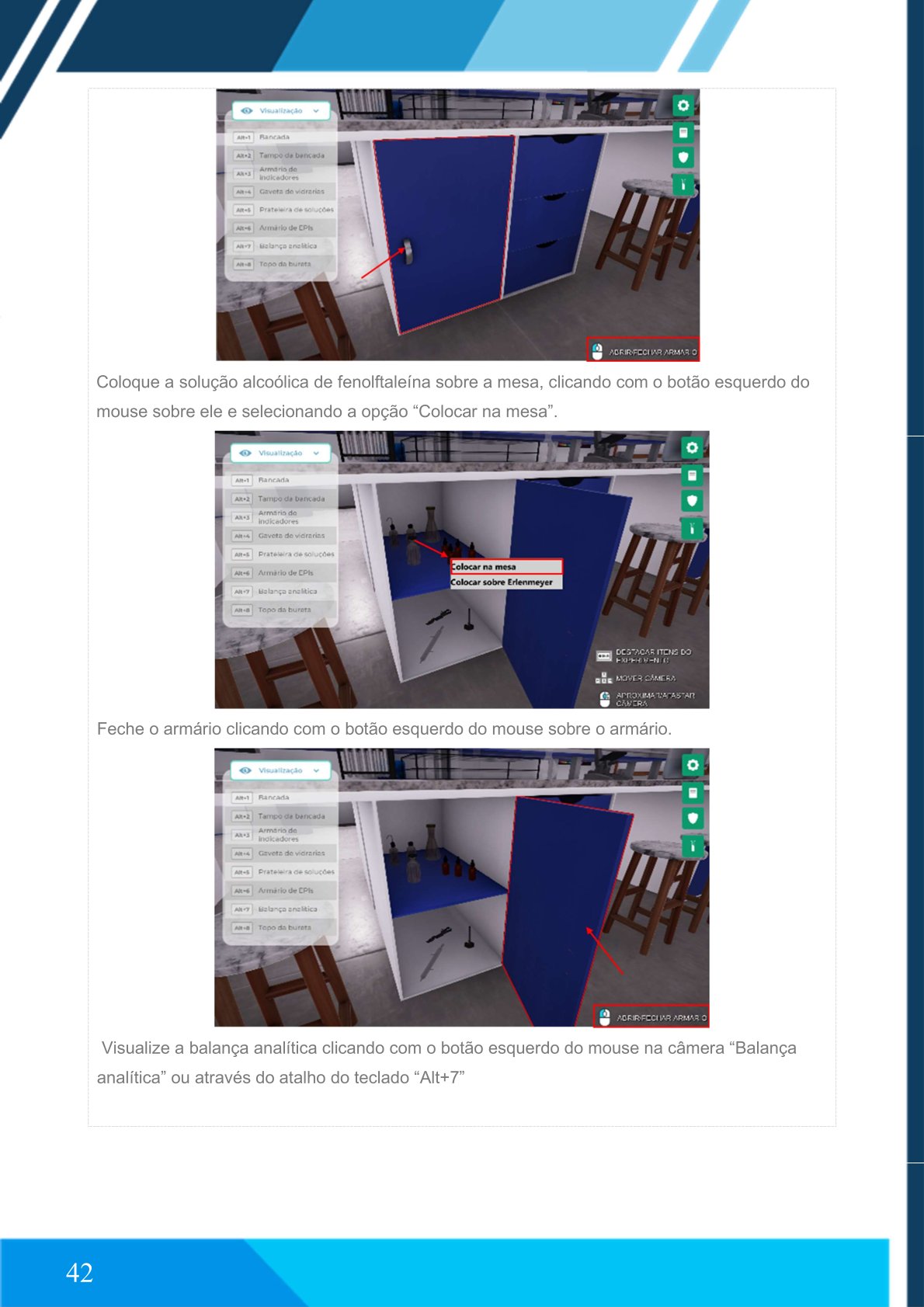
➨ Preparando a amostra para titulação
Dissolva o comprimido com água destilada e álcool etílico.
Misture a solução.
Adicione fenolftaleína.
Prepare o titulante (NaOH 0,1 mol/L) na bureta.
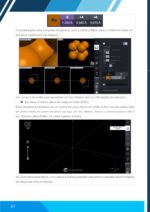
➨ Promovendo a titulação da amostra
Coloque o Erlenmeyer sob a bureta.
Abra a válvula lentamente.
Ao surgimento da coloração rosa, feche a válvula.
Anote o volume gasto.
Repita para obter a triplicata.
Calcule o teor de ácido acetilsalicílico.
➨ Finalizando o experimento
Esvazie e limpe:
Béquer
Proveta
Bureta
Erlenmeyer
➨ Avaliando os resultados
Preencha a tabela de dados do experimento e utilize as equações fornecidas.
Responda às questões propostas.
Checklist
✓ Acessar seu AVA
✓ Clicar no link do experimento REAÇÃO DE NEUTRALIZAÇÃO ÁCIDO-BASE
✓ Escolher o comprimido
✓ Garantir a segurança
✓ Preparar a amostra
✓ Promover a titulação
✓ Avaliar os resultados
RESULTADOS
Resultados de Aprendizagem:
Compreender como ocorre uma reação de neutralização, conhecer o processo titulométrico, usar a titulometria de neutralização e quantificar o ácido acetilsalicílico em amostras comerciais, além de conhecer as funcionalidades práticas das ferramentas do laboratório.
ESTUDANTE, VOCÊ DEVERÁ ENTREGAR
Ao final dessa aula prática, você deverá enviar um arquivo em Word contendo as informações obtidas no experimento, os cálculos realizados e um texto conclusivo.
O arquivo não pode exceder 2 Mb.
REFERÊNCIAS BIBLIOGRÁFICAS
Descrição (em ABNT) das referências utilizadas.
ROTEIRO DE AULA PRÁTICA 3
NOME DA DISCIPLINA: QUÍMICA E CIÊNCIA DOS MATERIAIS
Unidade: U3_ESTRUTURAS CRISTALINAS
Aula: A1_ESTRUTURAS CRISTALINAS E SISTEMAS CRISTALINOS
OBJETIVOS
(campo obrigatório – exibição para todos)
Compreender o ordenamento atômico de materiais que apresentam estrutura cristalina do tipo cúbica simples, cúbica de corpo centrado e cúbica de face centrada.
INFRAESTRUTURA
(OBRIGATÓRIO SE HOUVER – EXIBIÇÃO DOCENTE/TUTOR)
LABORATÓRIO DE INFORMÁTICA
Equipamentos:
• Computador com acesso à internet
~ 1 unidade / 1 aluno
SOLUÇÃO DIGITAL
(OBRIGATÓRIO SE HOUVER – APARECER PARA TODOS)
O CrystalWalk é um software livre que pode ser utilizado on-line e em dispositivos como computadores, tablets e smartphones.
Por meio dele, é possível construir estruturas cristalinas passo a passo e visualizar imagens tridimensionais, com comandos que possibilitam escolher estruturas básicas e os átomos que entrarão em sua composição.
EQUIPAMENTO DE PROTEÇÃO INDIVIDUAL (EPI)
(campo obrigatório – aparecer para todos)
Para a utilização do laboratório de informática não há necessidade de EPI’s.
PROCEDIMENTOS PRÁTICOS
(OBRIGATÓRIO – TODOS)
Procedimento / Atividade nº 1 (Virtual)
CONSTRUÇÃO DE CÉLULA UNITÁRIA DO TIPO CS, CCC E CFC
Atividade proposta:
Construir células unitárias e compreender como os átomos estão dispostos em estruturas cristalinas do tipo CS, CCC e CFC na formação de materiais.
Procedimentos para a realização da atividade
Em seu AVA, você irá encontrar o link do software CrystalWalk. A partir do acesso ao software, segue o procedimento a ser realizado para o desenvolvimento da atividade.
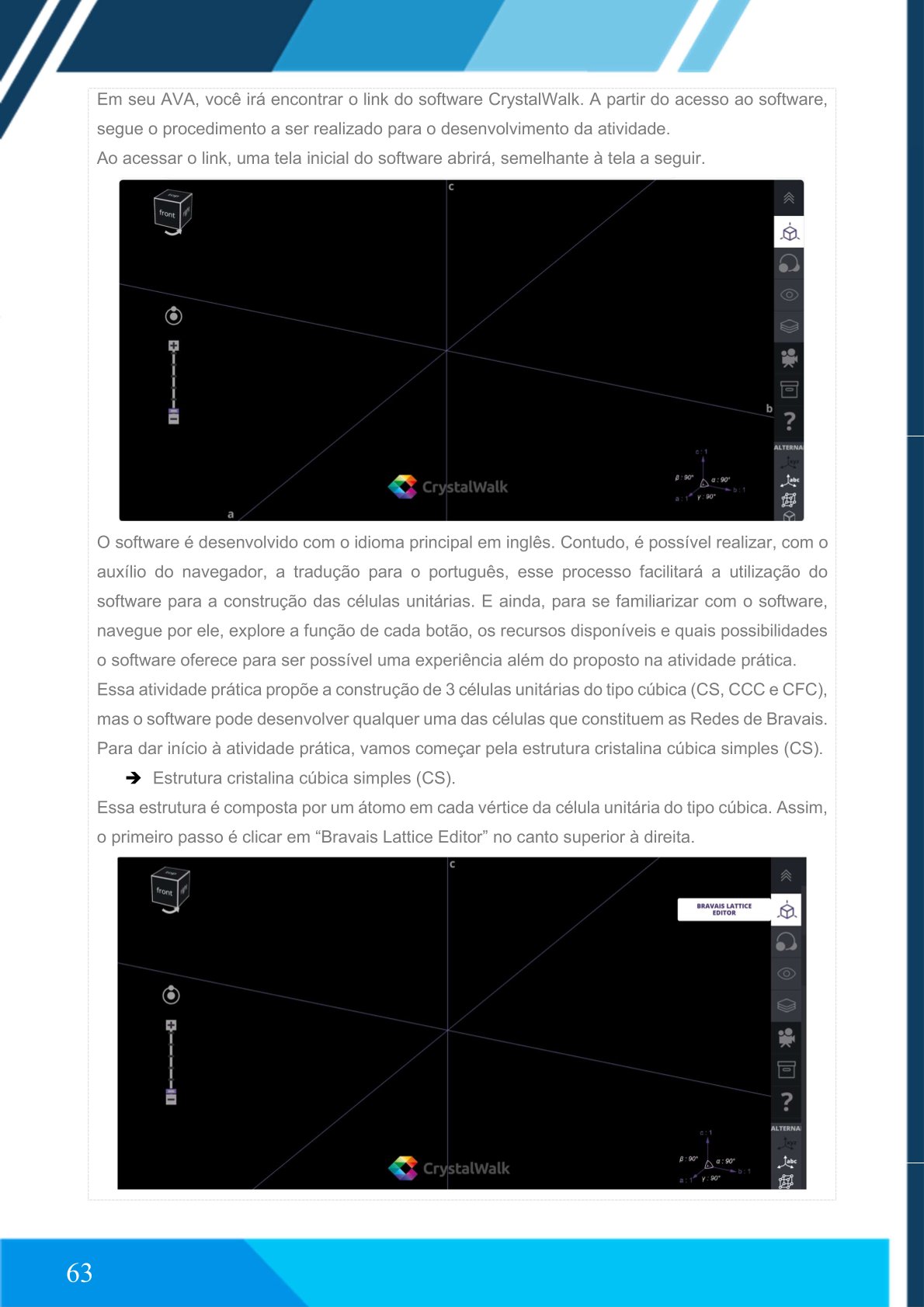
Ao acessar o link, uma tela inicial do software abrirá.
O software é desenvolvido em inglês, porém é possível utilizar a tradução automática do navegador para o português, facilitando sua utilização. Recomenda-se explorar as funções, botões e recursos disponíveis para melhor familiarização.
Esta atividade propõe a construção de três células unitárias do tipo cúbica (CS, CCC e CFC), embora o software permita construir qualquer célula das Redes de Bravais.
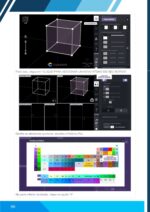
➨ Estrutura cristalina cúbica simples (CS)
Essa estrutura é composta por um átomo em cada vértice da célula unitária cúbica.
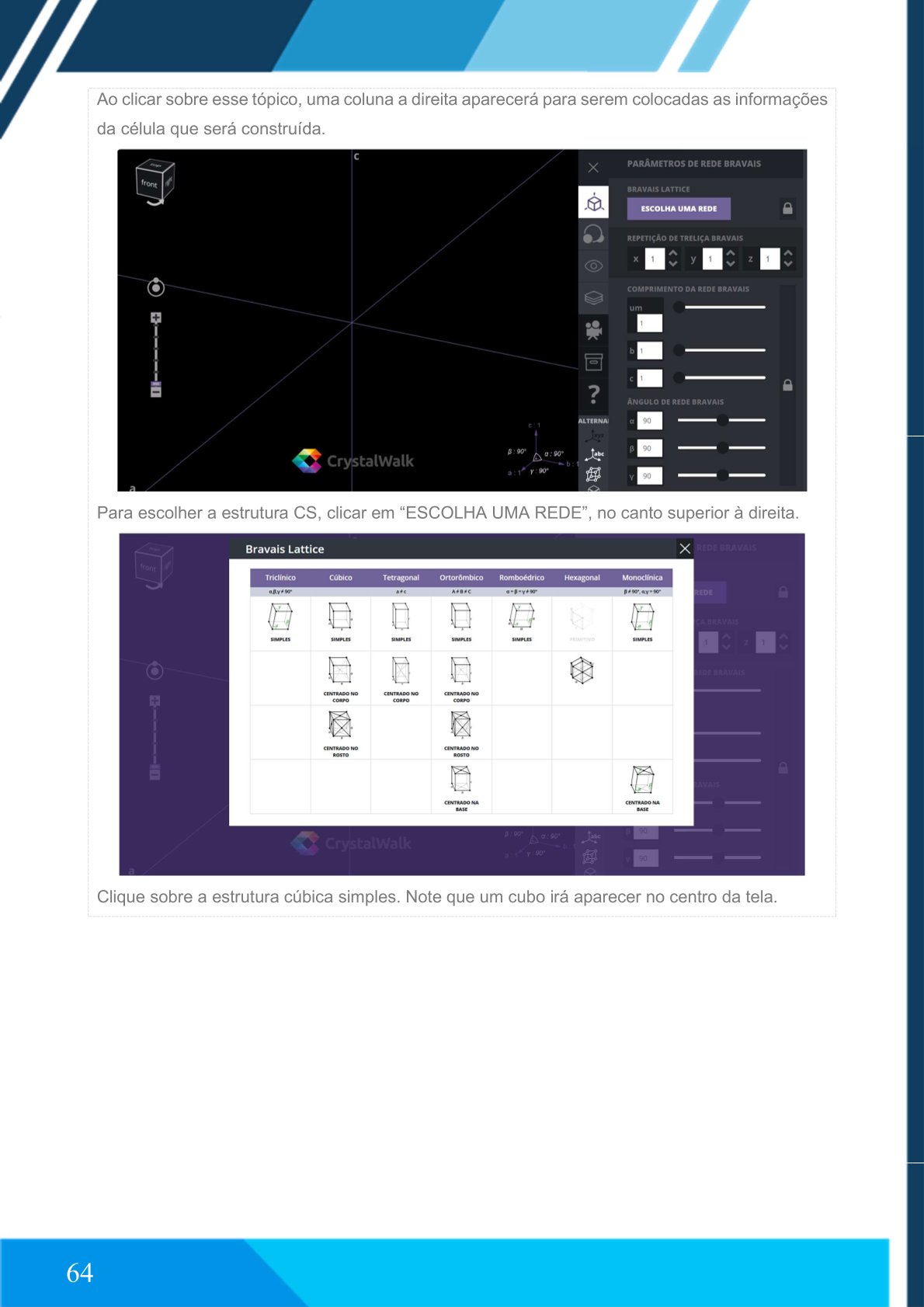
Clique em “Bravais Lattice Editor”.
Clique em “ESCOLHA UMA REDE” e selecione cúbica simples.
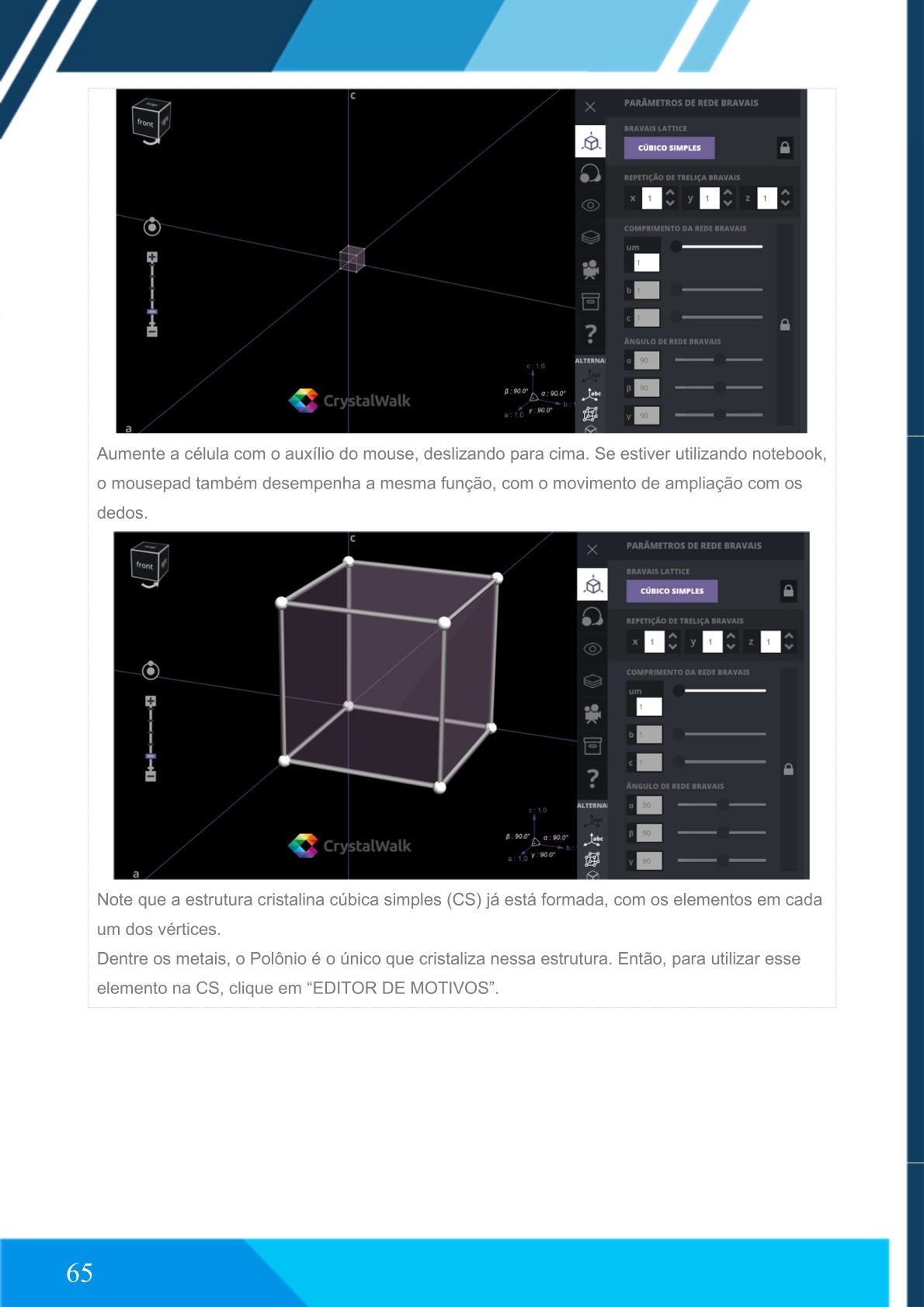
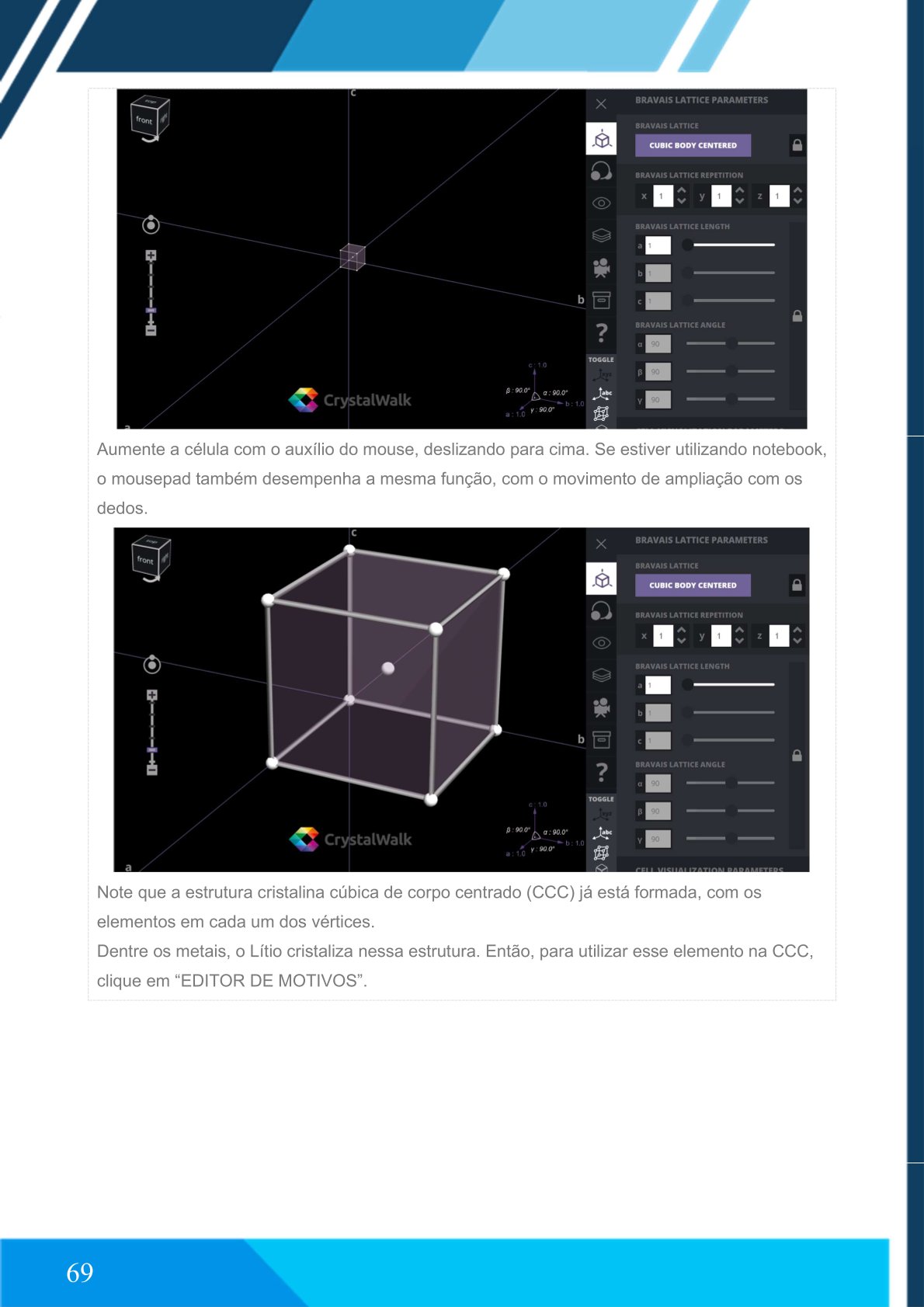
Aumente a célula com o auxílio do mouse.
Observe a estrutura formada.
Dentre os metais, o Polônio cristaliza nessa estrutura.
Clique em “EDITOR DE MOTIVOS”.
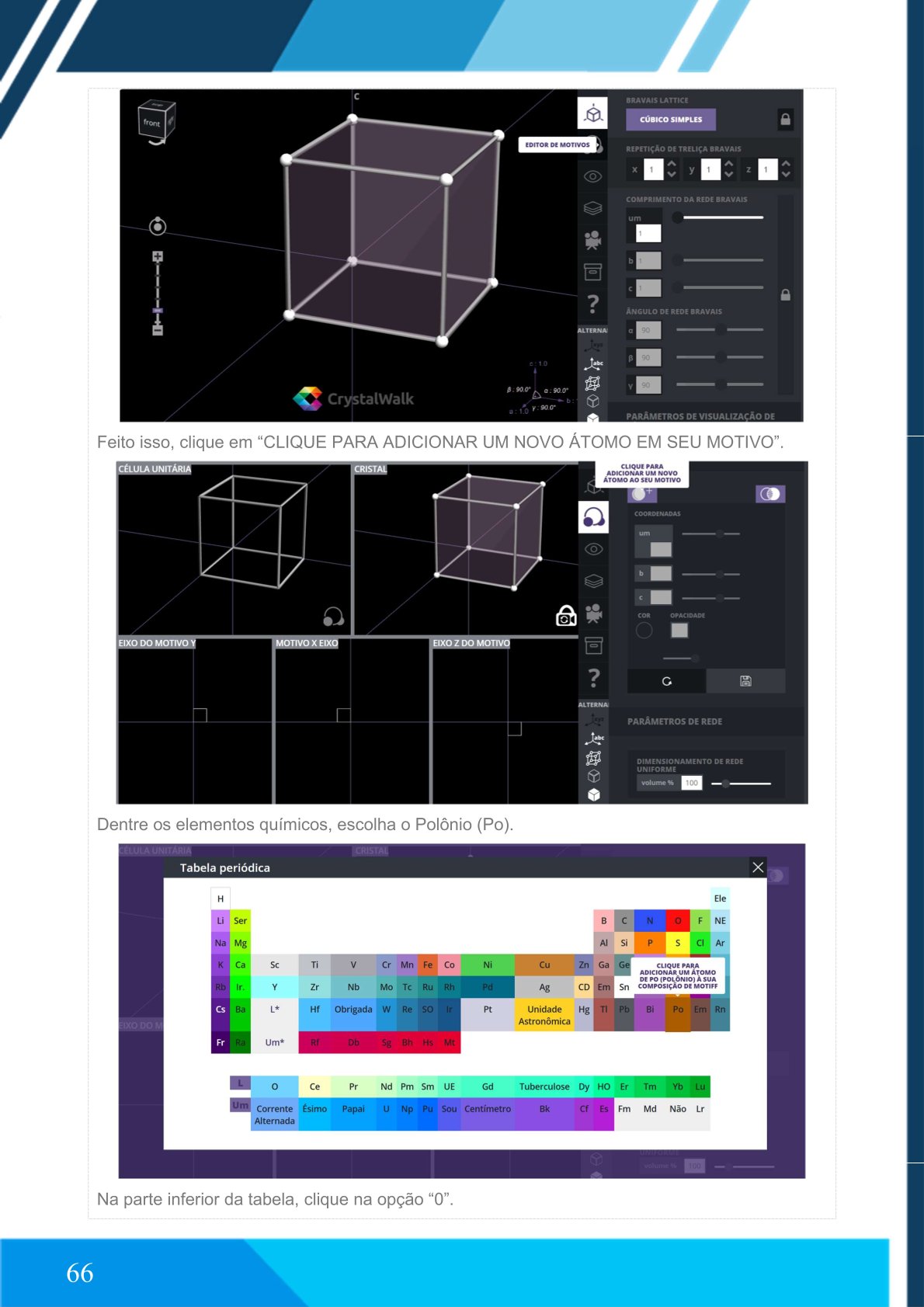
Clique em “CLIQUE PARA ADICIONAR UM NOVO ÁTOMO EM SEU MOTIVO”.
Escolha o elemento Polônio (Po).
Na parte inferior da tabela, clique na opção “0”.
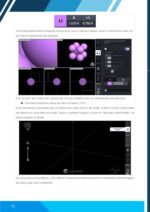
A estrutura aparecerá na célula unitária, no cristal e nos eixos cartesianos.
Tire um print para apresentar no relatório.
➨ Estrutura cristalina cúbica de corpo centrado (CCC)
Essa estrutura é composta por átomos nos vértices e um átomo no centro da célula.
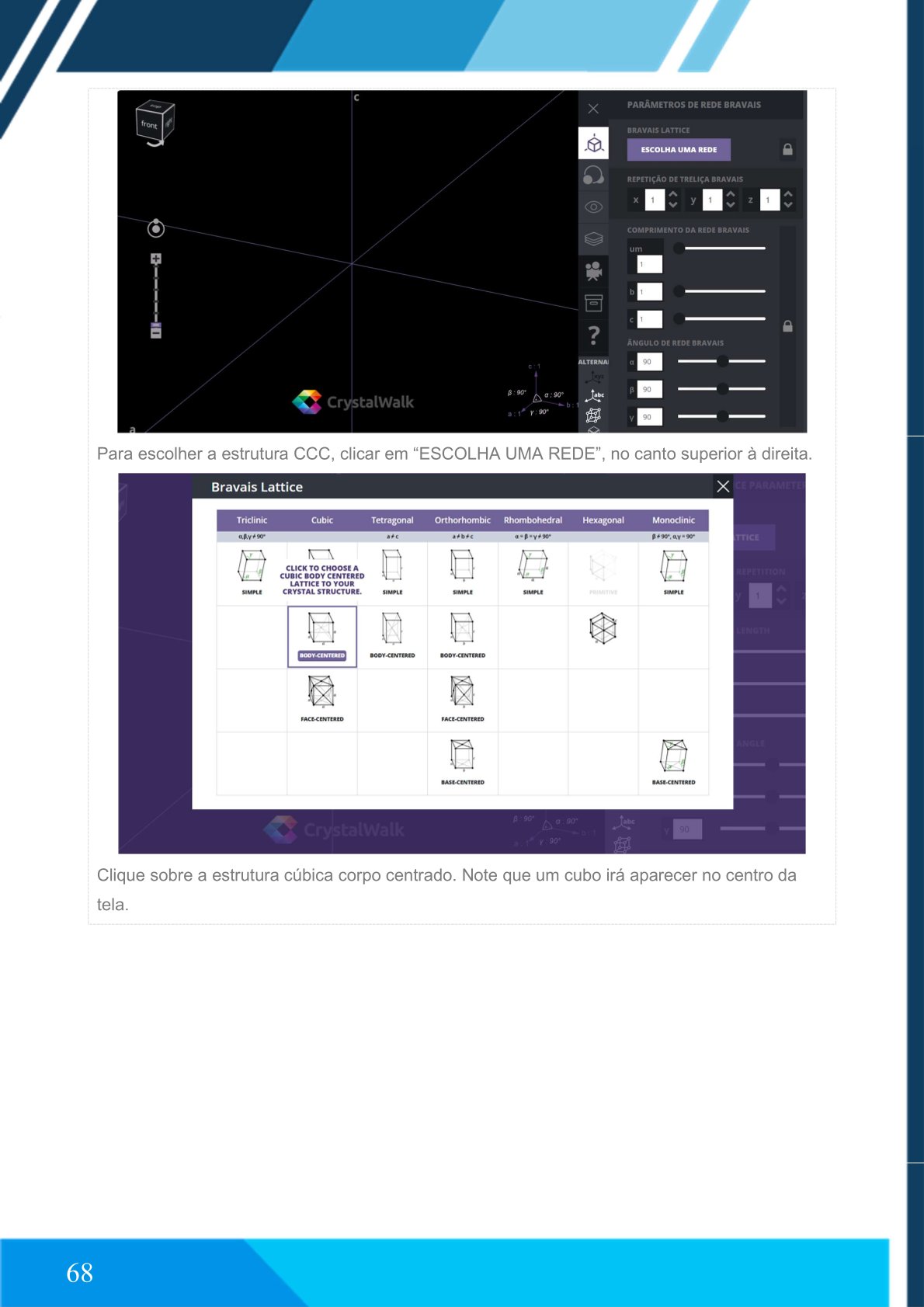
Clique em “Bravais Lattice Editor”.
Selecione cúbica corpo centrado em “ESCOLHA UMA REDE”.
Aumente a célula com o mouse.
O Lítio cristaliza nessa estrutura.
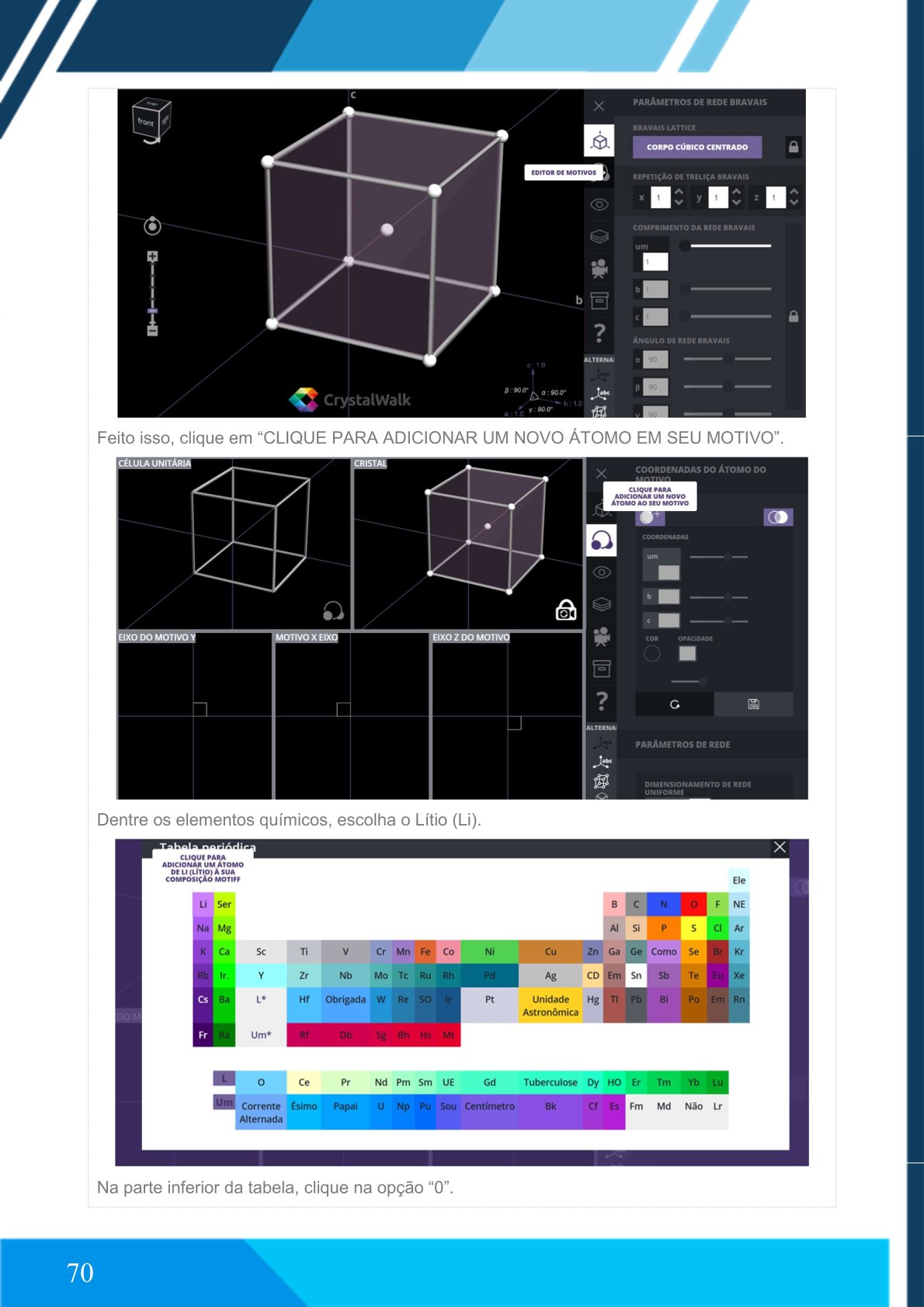
Clique em “EDITOR DE MOTIVOS”.
Clique em “CLIQUE PARA ADICIONAR UM NOVO ÁTOMO EM SEU MOTIVO”.
Escolha o elemento Lítio (Li).
Clique na opção “0” na tabela inferior.
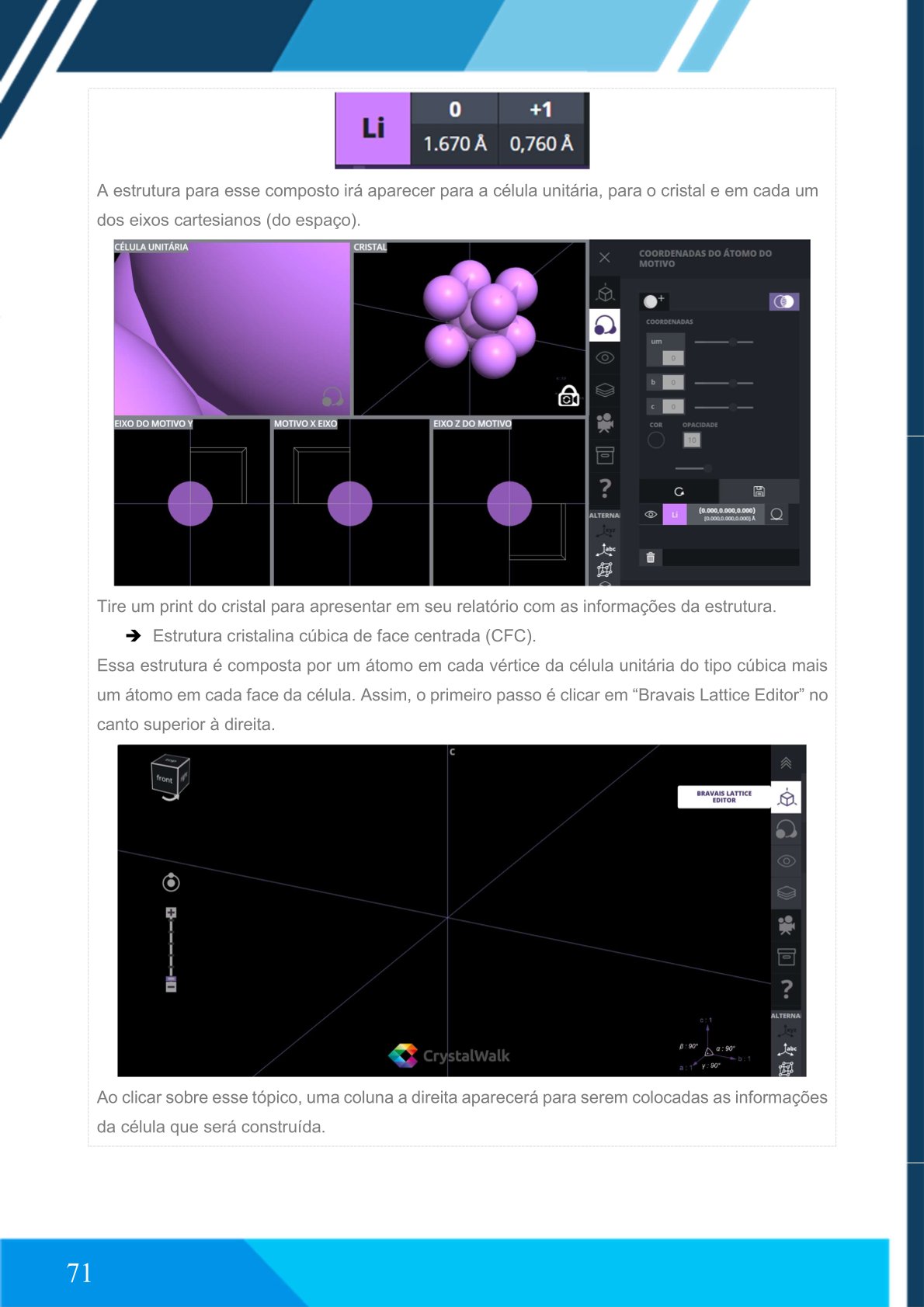
A estrutura será exibida na célula unitária, no cristal e nos eixos cartesianos.
Tire um print para o relatório.
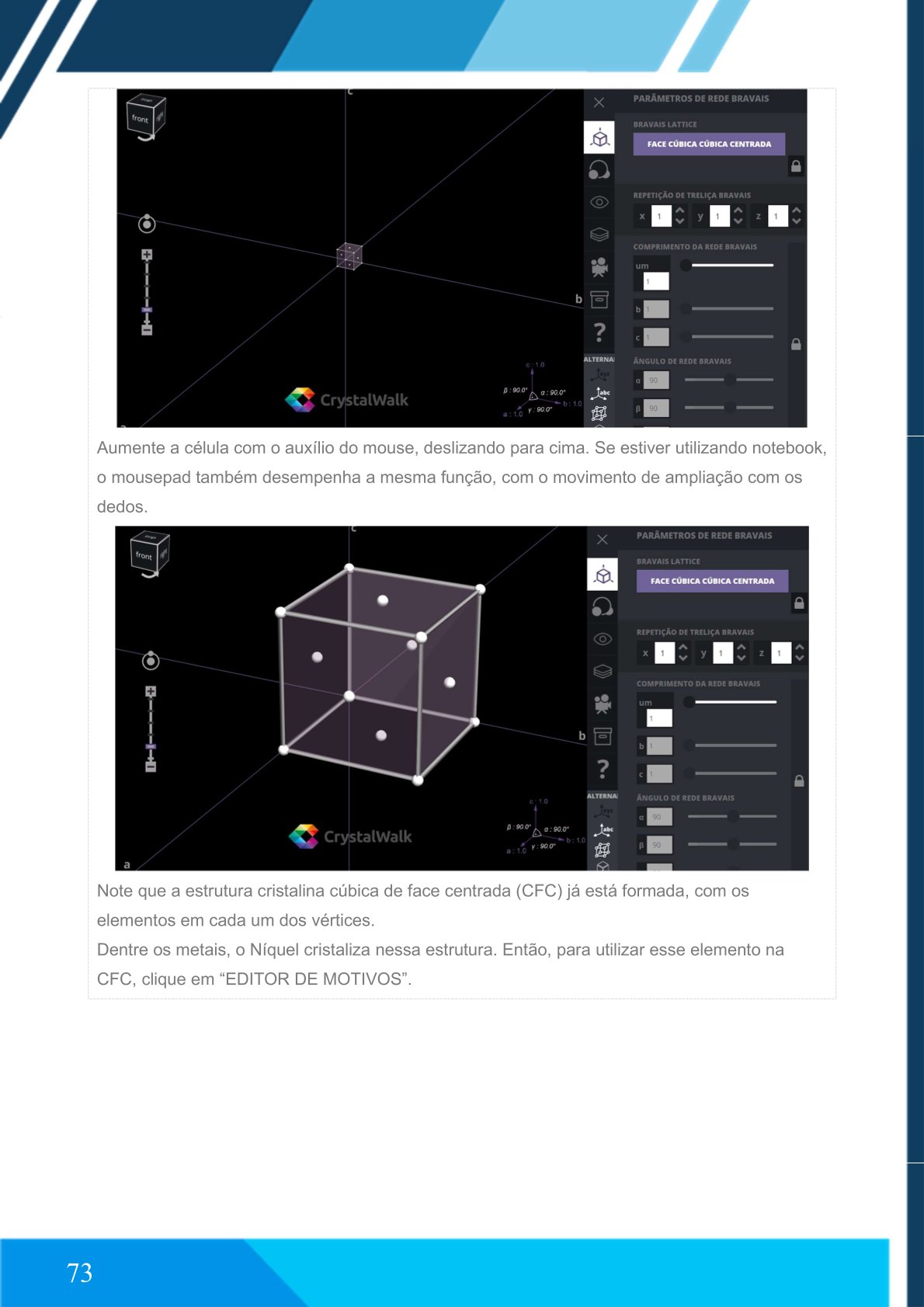
➨ Estrutura cristalina cúbica de face centrada (CFC)
Essa estrutura apresenta átomos nos vértices e no centro de cada face da célula.
Clique em “Bravais Lattice Editor”.
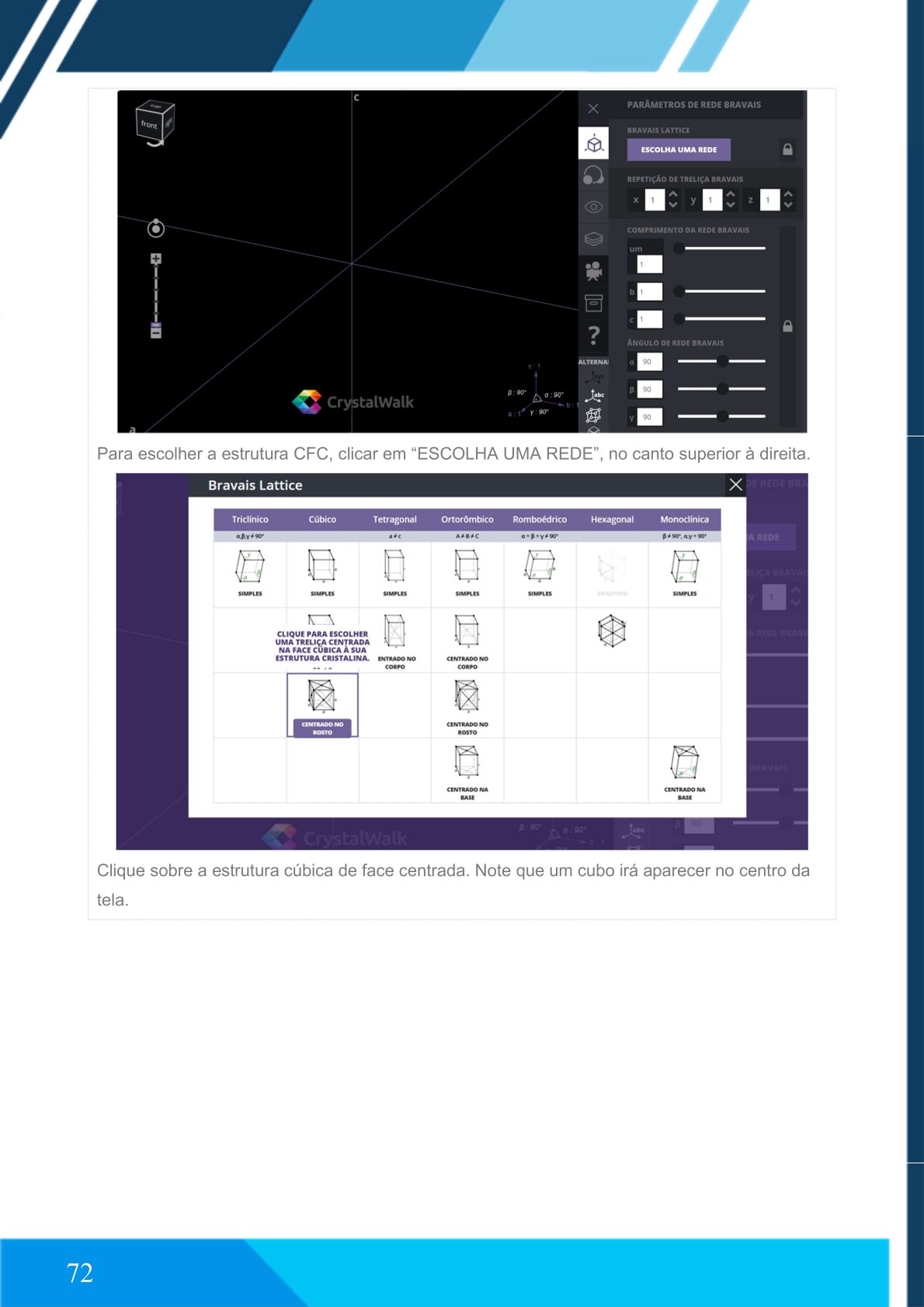
Selecione cúbica de face centrada.
Aumente a célula com o mouse.
O Níquel cristaliza nessa estrutura.
Clique em “EDITOR DE MOTIVOS”.
Clique em “CLIQUE PARA ADICIONAR UM NOVO ÁTOMO EM SEU MOTIVO”.
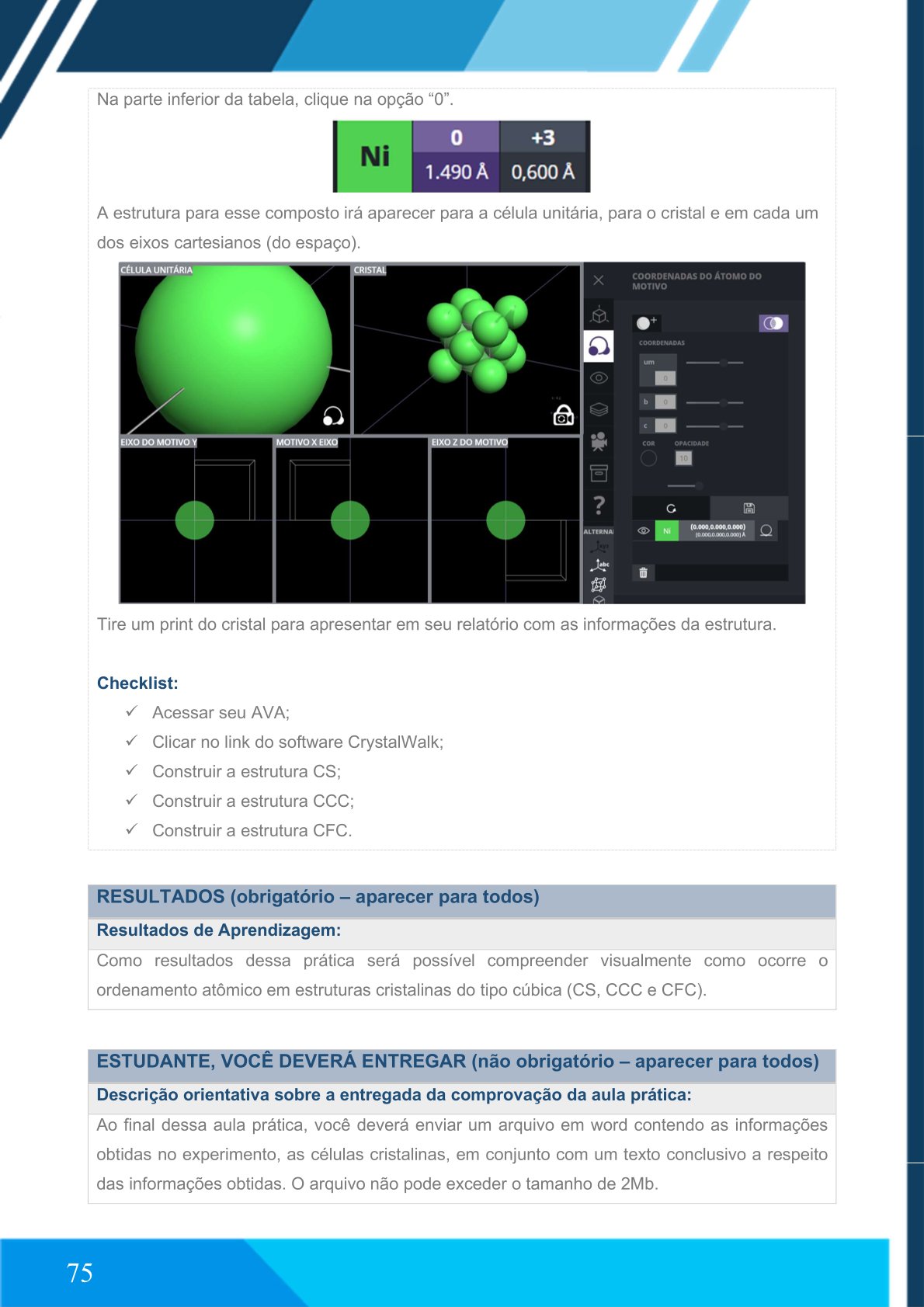
Escolha o elemento Níquel (Ni).
Clique na opção “0”.
A estrutura será exibida na célula unitária, no cristal e nos eixos cartesianos.
Tire um print para o relatório.
Checklist
✓ Acessar seu AVA
✓ Clicar no link do software CrystalWalk
✓ Construir a estrutura CS
✓ Construir a estrutura CCC
✓ Construir a estrutura CFC
RESULTADOS
(obrigatório – aparecer para todos)
Resultados de Aprendizagem:
Compreender visualmente como ocorre o ordenamento atômico em estruturas cristalinas do tipo cúbica (CS, CCC e CFC).
ESTUDANTE, VOCÊ DEVERÁ ENTREGAR
(não obrigatório – aparecer para todos)
Ao final dessa aula prática, você deverá enviar um arquivo em Word contendo as informações obtidas no experimento, as células cristalinas e um texto conclusivo.
O arquivo não pode exceder 2 Mb.
REFERÊNCIAS BIBLIOGRÁFICAS
(não obrigatório – aparecer para todos)
Descrição (em ABNT) das referências utilizadas.
ROTEIRO DE AULA PRÁTICA 4
NOME DA DISCIPLINA: QUÍMICA E CIÊNCIA DOS MATERIAIS
Unidade: U4_CLASSIFICAÇÃO E PROPRIEDADE DOS MATERIAIS
Aula: A1_MATERIAIS METÁLICOS
OBJETIVOS
(campo obrigatório – exibição para todos)
Analisar os dados de um ensaio de tração para obter as principais propriedades mecânicas do material.
INFRAESTRUTURA
LABORATÓRIO DE INFORMÁTICA
Equipamentos:
• Computador com acesso à internet
~ 1 unidade / 1 aluno
SOLUÇÃO DIGITAL
MDSolids – software educativo para estudo das propriedades e características de materiais e estruturas sob carregamento.
EQUIPAMENTO DE PROTEÇÃO INDIVIDUAL (EPI)
Para a utilização do laboratório de informática não há necessidade de EPI’s.
PROCEDIMENTOS PRÁTICOS
Procedimento / Atividade nº 1 (Virtual)
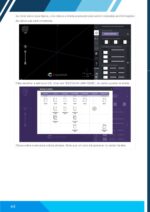
CONSTRUÇÃO DE UM DIAGRAMA TENSÃO / DEFORMAÇÃO
Atividade proposta:
Caracterizar um material por meio de suas propriedades mecânicas com base no diagrama tensão/deformação.
Procedimentos
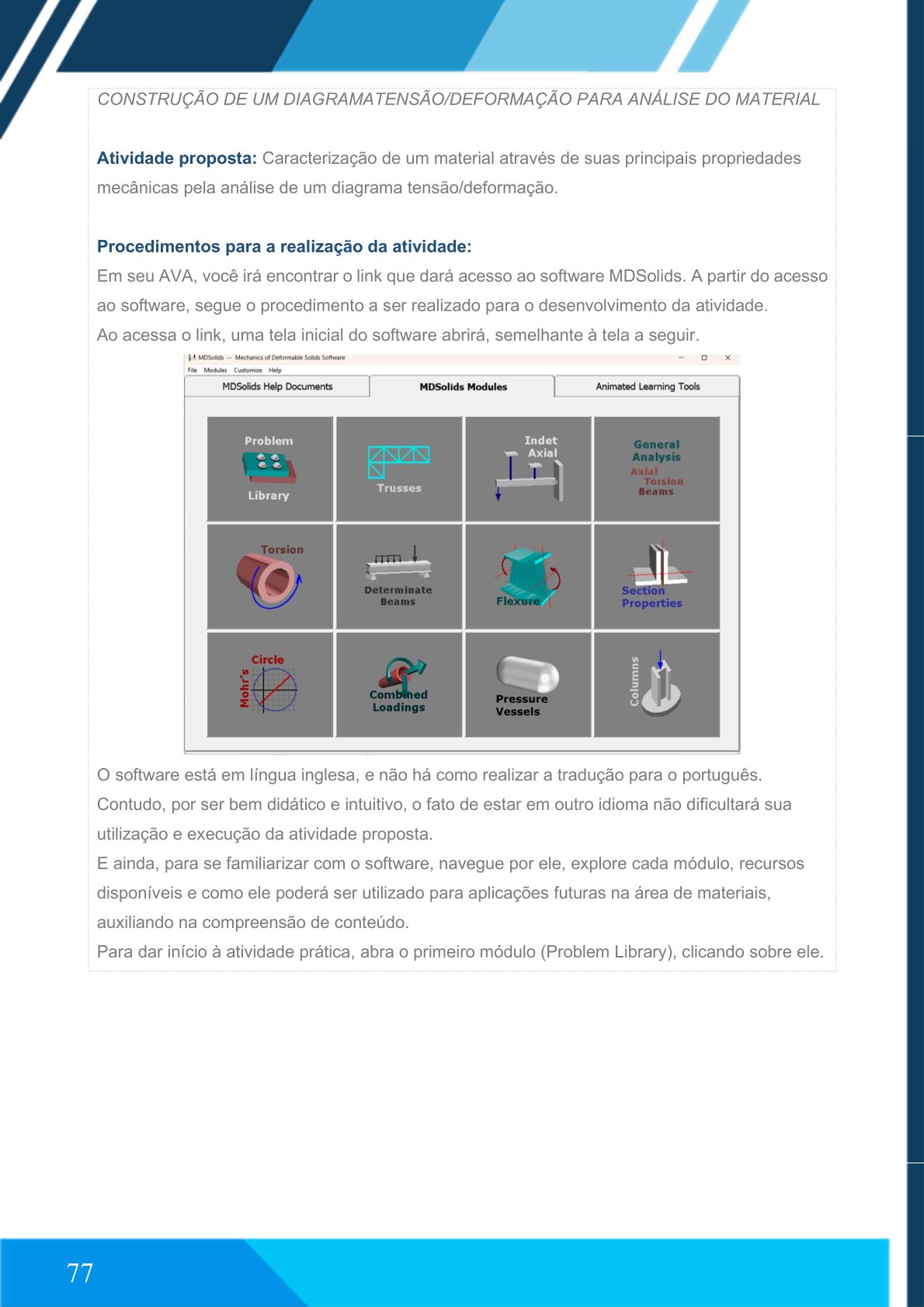
Acesse o software MDSolids pelo link disponível no AVA.
O software está em língua inglesa, porém é intuitivo e didático. Explore seus módulos e recursos.
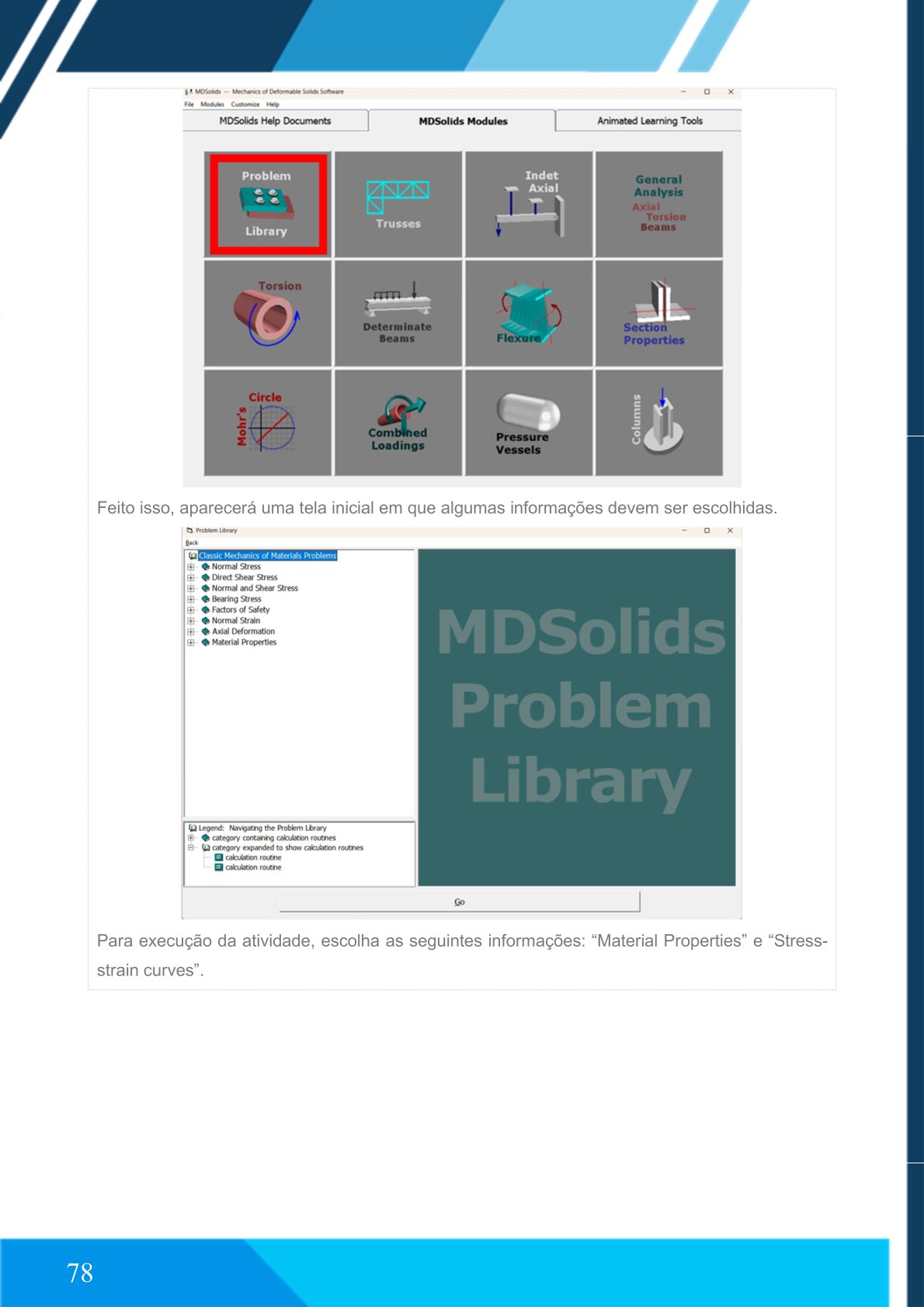
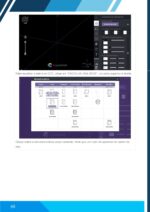
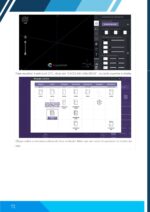
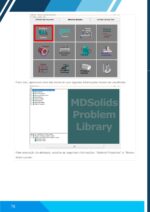
Abra o módulo Problem Library.
Selecione Material Properties e Stress-strain curves.
Clique em Go.
Insira os dados de força (N) e deformação (mm) fornecidos.
Configure as unidades:
Força: Newton (N)
Comprimento: milímetro (mm)
Tensão: MPa
Deformação: mm/mm
Considere:
Gage length: 300 mm
Área: 7,07 mm²
Ajuste a tabela para 25 linhas e clique em Plot.
➨ Avaliando os resultados
Responda:
O material é dúctil ou frágil? Por quê?
Quais os valores de tensão máxima e de ruptura?
É possível calcular o módulo de elasticidade? Qual o valor?
Checklist
✓ Acessar o AVA
✓ Acessar o software
✓ Utilizar o módulo Problem Library
✓ Inserir os dados
✓ Plotar o diagrama
✓ Avaliar os resultados
RESULTADOS
Resultados de Aprendizagem:
Compreender como construir e analisar um diagrama tensão/deformação para obtenção das principais propriedades mecânicas do material.
ESTUDANTE, VOCÊ DEVERÁ ENTREGAR
Arquivo em Word com os dados obtidos, cálculos realizados e texto conclusivo.
Tamanho máximo: 2 Mb.
REFERÊNCIAS BIBLIOGRÁFICAS
Descrição (em ABNT) das referências utilizadas.
Produtos relacionados
ROTEIRO AULA PRÁTICA – DESENVOLVIMENTO MOBILE
Em até 12x de R$10,69
ROTEIRO AULA PRÁTICA – PROTOCOLO DE REDES
Em até 12x de R$10,69
ROTEIRO AULA PRÁTICA – SISTEMAS DIGITAIS E MICROPROCESSADORES
Em até 12x de R$10,69
ROTEIRO DE AULA PRÁTICA – ESTATÍSTICA DE DADOS AMBIENTAIS
Em até 12x de R$10,69
ROTEIRO DE AULA PRÁTICA – FENÔMENOS DE TRANSPORTE
Em até 12x de R$10,69
ROTEIRO DE AULA PRÁTICA – FÍSICA GERAL E EXPERIMENTAL: ENERGIA
Em até 12x de R$10,69
ROTEIRO DE AULA PRÁTICA – FUNDAMENTOS DE CARTOGRAFIA E TOPOGRAFIA
Em até 12x de R$11,88